

M.D.
numero 14, 25 aprile 2007
Clinica
Calcolosi urinaria: diagnosi e terapia
di Ciro Niro,* Giovanni Battista D’Errico,** Nunzio
Costa***
* Medico di medicina generale, San Severo (FG), Responsabile
Nazionale Dipartimento Uro-Andologia AIMEF
** Medico di medicina generale, Foggia, Responsabile Nazionale
Dipartimento Oncologia e Cure Palliative AIMEF
*** Medico di medicina generale, Stornarella (FG), AIMEF
La presente rassegna fa riferimento alla recente revisione
delle linee guida sulla calcolosi urinaria promossa dalla Associazione
Urologi Italiani (AURO.it). Viene proposto un aggiornamento
dei capitoli di inquadramento diagnostico e intervento terapeutico
che coinvolgono direttamente l’operato e le scelte del
medico di famiglia
Gli
studi epidemiologici mostrano che l’urolitiasi è
un disturbo frequente che colpisce il 20% degli uomini e il
10% delle donne, principalmente nella fascia di età tra
i 20 e i 40 anni. Un fatto curioso è che circa il 20%
dei medici ha avuto un episodio di colica ureterale.
L’incidenza varia notevolmente nelle differenti popolazioni
e nei Paesi occidentali si è assistito a un sensibile
aumento interrotto solo dalle due guerre mondiali, dato da cui
si è ricavato che l’incidenza della calcolosi è
più elevata nei Paesi socialmente più evoluti,
dove le condizioni di vita e soprattutto l’alimentazione
sono migliori.
La frequenza della patologia litiasica impone un iter diagnostico
essenziale, rapido e con costi contenuti.
Il paziente litiasico giunge all’osservazione del medico
di famiglia per i sintomi o per un riscontro casuale del
calcolo. In caso di colica reno-ureterale isolata o di reperto
incidentale non sussistono criteri di urgenza e il paziente
può essere inquadrato anche ambulatorialmente.
Quando invece i sintomi sono subentranti o incoercibili, si
rende necessaria l’ospedalizzazione per una rapida diagnosi
e talora soluzione terapeutica in tempi brevi, anche per evitare
e/o risolvere le complicazioni dell’ostruzione.
L’iter diagnostico della calcolosi si articola in più
livelli con grado crescente di approfondimento morfologico e
metabolico.
Diagnosi iniziale
Anamnesi
La diagnosi iniziale della calcolosi urinaria si basa su una
dettagliata raccolta anamnestica per fare emergere tutti quei
fattori di rischio correlati alla formazione di calcoli e alle
complicanze derivanti dalla urolitiasi.
Familiarità
L’aumentata frequenza di litiasi in alcune famiglie potrebbe
essere interpretata come una tendenza ereditaria a formare
calcoli, che insorge solo quando diversi fattori, quali abitudini
alimentari (per es. ridotta introduzione di calcio nella dieta)
e ambientali, si associano.
La familiarità sarebbe invece inversamente correlata
alla formazione “attiva” dei calcoli, cioè
a un aumento del numero, delle dimensioni dei calcoli o ad una
ricorrenza entro i due anni.
Il fenotipo riscontrato più frequentemente in famiglie
con almeno due fratelli affetti da calcolosi calcica sembra
essere quello associato a ipercalciuria; il fatto che l’escrezione
urinaria di calcio, nell’ambito della stessa famiglia,
sia differente tra i soggetti con urolitiasi e quelli senza,
suggerisce l’ereditarietà, anche se non la prova,
e che teoricamente l’ipercalciuria potrebbe essere legata
a fattori ambientali non identificati.
Patologie urologiche concomitanti
In oltre il 30% dei casi si possono riscontrare patologie urologiche
concomitanti alla calcolosi urinaria e rappresentate da: diverticolosi
caliciale, rene a spugna midollare, cisti renali, duplicità
ureterale, stenosi uretrali, rene a ferro di cavallo, stenosi
del giunto pielo ureterale, ureterocele, tubercolosi urinaria.
Allo stesso modo precedenti episodi di litiasi possono rappresentare
fattori di rischio per la recidiva di calcoli fino a circa il
57% dei casi.
Importanti fattori di rischio per la litiasi urinaria sono:
ipercalciuria, ipocitraturia, iperossaluria, iperuricuria e
infezioni delle vie urinarie (UTI) ricorrenti.
Anche un aumento dell’azoturia, come risultato di un maggiore
introito proteico, può rappresentare un fattore di rischio.
La vasectomia determinerebbe un rischio relativo raddoppiato
di urolitiasi, in soggetti di età >46 anni e fino
a 14 anni dopo l’intervento.
Patologie non urologiche concomitanti
Le malattie infiammatorie intestinali (morbo di Crohn e rettocolite)
con o senza resezione intestinale, si associano a un’incidenza
di calcolosi dal 5% al 25% nei diversi studi.
Soggetti con morbo di Crohn manifestano ipocitraturia, ipomagnesuria
e ridotto volume di urine a pH acido. Allo stesso modo, pazienti
sottoposti a resezione intestinale, specialmente dopo ileostomia,
presentano ridotto volume di urine a pH acido, ridotta escrezione
urinaria di magnesio, citrato, sodio, elevata concentrazione
di ossalato, calcio e acido urico con iperuricemia; tutto ciò
può portare alla formazione di calcoli di ossalato di
calcio e acido urico.
L’iperparatiroidismo si associa frequentemente a un più
alto contenuto medio di urato di ammonio e quindi alla calcolosi.
Il diabete mellito, l’ipertensione arteriosa, la cardiopatia
ischemica e l’ulcera peptica si associano a una maggiore
prevalenza della malattia litiasica, ma senza una significatività
statistica.
 Terapie
concomitanti Terapie
concomitanti
I calcoli indotti da farmaci rappresentano l’1-2% del totale;
essi possono essere suddivisi in due gruppi a seconda del meccanismo
inducente la litiasi.
Al primo gruppo appartengono i farmaci poco solubili che cristallizzano
nelle urine; il secondo gruppo comprende farmaci con effetto
metabolico.
Bisogna tuttavia considerare che intervengono anche particolari
e concomitanti fattori di rischio legati al paziente, quali
il pH e il volume urinario (tabella 1) e al farmaco stesso (tabella
2).
Trattamento del dolore
La colica reno-ureterale è una frequente causa di dolore
severo, debilitante, e richiede un pronto e adeguato trattamento:
gli obiettivi della terapia sono eliminare il dolore, facilitare
l’espulsione del calcolo e preservare la funzione renale
dal danno causato dalla prolungata ostruzione.
I cambiamenti biochimici che intervengono negli stadi iniziali
della colica comprendono il rilascio locale di sostanze vasoattive
che agiscono principalmente sui vasi preglomerulari. Sostanze
come prostacicline (PGI2), prostaglandine (PGE2) e ossido nitrico
(NO) causano vasodilatazione con aumento del filtrato glomerulare
(FG) e della pressione intraureterale.
 Successivamente
però si attiva un meccanismo compensatorio: una vasocostrizione
connessa a riduzione del filtrato glomerulare, mediata da endotelina,
angiotensina II e trombossano, induce una riduzione della pressione
intraureterale. L’ormone antidiuretico (ADH) contribuisce
a ridurre ulteriormente il volume urinario. Successivamente
però si attiva un meccanismo compensatorio: una vasocostrizione
connessa a riduzione del filtrato glomerulare, mediata da endotelina,
angiotensina II e trombossano, induce una riduzione della pressione
intraureterale. L’ormone antidiuretico (ADH) contribuisce
a ridurre ulteriormente il volume urinario.
I potenziali rischi correlati alla somministrazione di diuretici
o di elevati volumi di liquidi (rottura della via escretrice
e/o danno irreversibile della funzione renale) sono superiori
ai potenziali benefici, peraltro non univocamente dimostrati.
L’infusione endovenosa di liquidi è utile solo in
pazienti disidratati, per il vomito o un’eccessiva
restrizione idrica, al fine di mantenere un corretto bilancio
idroelettrolitico.
Sono vari i farmaci che vengono adoperati per il controllo del
dolore nella colica renale.
FANS
I FANS rappresentano oggi la terapia di prima scelta. La loro
azione si esplica attraverso la riduzione della risposta flogistica,
dell’edema locale e del flusso ematico renale con riduzione
del filtrato glomerulare fino al 35%; inoltre essi riducono
la peristalsi ureterale per effetto miorilassante diretto e
per una diminuzione della pressione intraureterale successiva
al calo del filtrato glomerulare.
Essi agiscono principalmente inibendo l’attività
della ciclossigenasi (COX) che regola la sintesi delle prostaglandine
e del trombossano.
Sono conosciute tre classi di FANS in rapporto alla loro inibizione
della COX: non selettivi, inibitori COX 1 selettivi, inibitori
COX 2 selettivi (controindicati nei pazienti con danno renale
perché riducono ulteriormente il FG).
La loro somministrazione va evitata in caso di ulcera peptica
conosciuta, insufficienza renale e gravidanza; deve essere effettuata
con cautela nei pazienti più anziani, con diabete, ipertensione
e in caso di disidratazione.
Due trial clinici randomizzati hanno confrontato l’efficacia,
in termini di riduzione soggettiva e oggettiva del dolore, del
ketorolac rispetto agli spasmolitici e agli oppiacei: le conclusioni
hanno dimostrato che l’aggiunta dello spasmolitico al FANS
non porta ad alcun effetto aggiuntivo o sinergico sul controllo
del dolore. Rispetto agli oppiacei il ketorolac porta a un maggior
sollievo del dolore e, anche se non in maniera statisticamente
significativa, riduce i tempi di dimissione ospedaliera dei
pazienti affetti da colica renale da litiasi.
Oppiacei analgesici
Gli oppiacei analgesici esplicano la loro azione impedendo l’entrata
di ioni calcio nelle cellule nervose e riducendo così
i livelli cerebrali di calcio; questi bassi livelli di calcio
intracellulare nei neuroni bersaglio degli oppiacei analgesici
riducono il rilascio di neurotrasmettitori (ACTH, noradrenalina,
serotonina e sostanza P) e di conseguenza viene ridotta l’attivazione
dei siti post-sinaptici. È stato recentemente ipotizzato
che gli effetti degli oppiacei analgesici siano anche correlati
agli inibitori dell’adenilato ciclasi.
Perifericamente essi agiscono direttamente sulla muscolatura
liscia ureterale con aumento della lunghezza e del tono delle
contrazioni isotoniche e ciò porta a uno spasmo ureterale
che aumenta la pressione intra-ureterale e costituisce un ostacolo
alla progressione ed eliminazione del calcolo.
Gli oppiacei inoltre non trattano la causa del dolore e possono
indurre, oltre a dipendenza, effetti collaterali e da considerarsi
di seconda scelta nella colica renale.
Spasmolitici
Gli studi presenti in letteratura sull’uso degli spasmolitici
sono scarsi e contrastanti tra loro, per cui mentre da un lato
si dimostra che l’uso di uno spasmolitico quale la drotaverina
(non in commercio in Italia), che agirebbe bloccando la fosfodiesterasi
IV delle cellule muscolari lisce, ha una efficacia molto alta,
con riduzione del dolore in più dei 2/3 dei casi, all’opposto,
in un altro studio si è concluso che gli spasmolitici-anticolinergici,
che agiscono inibendo gli effetti muscarinici dell’acetilcolina,
aggiunti ai FANS, non hanno determinato alcun effetto aggiuntivo
né sinergico, rispetto a questi ultimi utilizzati da
soli, sul controllo del dolore nella colica renale.
Questa mancanza di prova di efficacia potrebbe essere legata
o alla assenza di recettori muscarinici a livello ureterale
o al fatto che l’effetto anticolinergico di queste sostanze
viene mascherato da quello antiprostaglandinico dei FANS.
Altri trattamenti
-
ADH:
agisce attraverso un potente effetto anti-diuretico con rilassamento
della pelvi renale e della muscolatura liscia ureterale, ma
ha una breve durata d’azione (30 minuti).
-
Agopuntura
e anestesia loco-regionale: l’agopuntura aumenta gli
oppioidi endogeni come beta-endorfina nel sistema nervoso
centrale (ciò modifica gli impulsi afferenti nella
corda spinale).
L’anestesia
locale T11-L1 blocca la trasmissione del segnale doloroso.
Inquadramento diagnostico con metodiche di imaging
La diagnostica per immagini gioca un ruolo fondamentale nel
trattamento dei pazienti con calcolosi urinaria. In presenza
di tale sospetto clinico è necessario intraprendere un
iter diagnostico che valuti:
1. presenza o assenza della litiasi;
2. sede, dimensioni, numero e natura del calcolo;
3. presenza di eventuali segni secondari come ostruzione delle
vie escretrici;
4. valutazione della funzionalità renale ed escretrice
omolaterale e controlaterale;
5. eventuale infezione associata;
6. eventuale associazione di malformazioni urinarie;
7. capacità di progressione del calcolo.
Un’analisi preliminare consentirà di accertare la
presenza della calcolosi, mentre il passo immediatamente successivo
avrà come obiettivo la definizione del grado di severità
della malattia tramite metodiche in grado di valutare non solo
la sede, le dimensioni, la forma, il numero e la natura del
calcolo insieme alle probabilità di espulsione spontanea,
ma anche la sofferenza renale che può derivare dall’eventuale
ostruzione delle vie escretrici con conseguente riduzione della
funzionalità dell’organo.
 Le
informazioni che vengono richieste alle varie tecniche per imaging
servono quindi a stabilire l’iter terapeutico successivo:
l’evidenziazione di un’ostruzione significativa con
progressivo deterioramento della funzione renale ci orienterà,
per esempio, verso una terapia procedurale d’urgenza anziché
verso la programmazione di un trattamento di elezione. Le
informazioni che vengono richieste alle varie tecniche per imaging
servono quindi a stabilire l’iter terapeutico successivo:
l’evidenziazione di un’ostruzione significativa con
progressivo deterioramento della funzione renale ci orienterà,
per esempio, verso una terapia procedurale d’urgenza anziché
verso la programmazione di un trattamento di elezione.
Tutte le metodiche di imaging a disposizione hanno il loro ruolo
individuale da giocare, con alcuni limiti, ma comunque devono
fornire, nel caso di sospetta patologia calcolotica, precise
informazioni: stabilire la diagnosi di calcolosi; determinare
la sede del calcolo; evidenziare l’anatomia pelvico-caliceale;
valutare la funzionale renale; programmare la terapia (litrotrissia,
nefrolitotomia percutanea, laparoscopia, ecc) e valutare i risultati
della terapia.
Da questo nasce la necessità di valutare i tratti della
via escretrice dove si hanno cambiamenti di diametro del lume
del canale escretorio, e dove si può incuneare il calcolo:
colletto di un calice; giunzione pielo-ureterale; incrocio con
i vasi iliaci; pelvi posteriore; giunzione uretero-vescicale.
 È
chiaro che le informazioni sulla sede, integrate con gli altri
dati (dimensioni, natura, complicazioni), orientano sulla capacità
di progressione del calcolo e sulla procedura terapeutica più
opportuna, notizie fornite, in caso di positività per
calcolosi, nella maggioranza dei casi da indagini basali dell’imaging
diagnostico, eseguibili velocemente anche in condizioni di emergenza
(tabella 3). È
chiaro che le informazioni sulla sede, integrate con gli altri
dati (dimensioni, natura, complicazioni), orientano sulla capacità
di progressione del calcolo e sulla procedura terapeutica più
opportuna, notizie fornite, in caso di positività per
calcolosi, nella maggioranza dei casi da indagini basali dell’imaging
diagnostico, eseguibili velocemente anche in condizioni di emergenza
(tabella 3).
Qualsiasi dubbio riguardo al grado dell’ostruzione e alla
compromissione funzionale impone il passaggio a un livello di
indagine superiore con l’intento di definire, oltre al
quadro ostruttivo, l’entità del danno e le capacità
di recupero della funzionalità renale e valutare lo stato
del rene controlaterale.
La valutazione funzionale sarà importante soprattutto
in presenza di una storia di calcoli multipli con associata
infezione e/o di pregressi interventi per rimuoverli.
Il passaggio spontaneo del calcolo attraverso le vie escretrici
renali è in rapporto alle sue dimensioni: un calcolo
di 1 mm di diametro ha circa l’87% di probabilità
di essere espulso spontaneamente, un calcolo di 7-9 mm di diametro
ha solo il 25% di probabilità. Ma questo dipende anche
dalla sua localizzazione: 48% in sede prossimale, 60% in sede
mediale e 75% in sede distale.
Le dimensioni del calcolo sono fondamentali per l’eventuale
trattamento: infatti calcoli >6 mm solitamente necessitano
di trattamento per improbabile espulsione spontanea, quelli
di dimensioni tra i 4 e i 6 mm presentano una probabile espulsione
spontanea, quelli <4 mm vengono solitamente espulsi spontaneamente
entro 3 mesi.
La risposta a queste domande è fornita dalle metodiche
di imaging a disposizione.
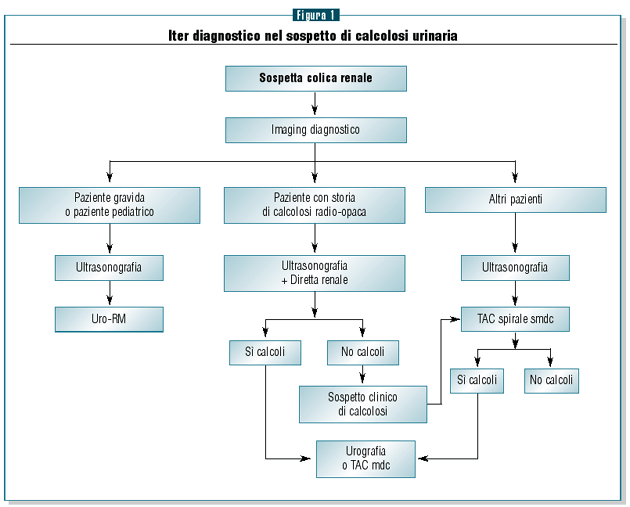
Nel sospetto di calcolosi urinaria l’iter diagnostico suggerito,
che schematicamente è riassunto in figura 1, non deve
essere tuttavia considerato limitativo, in quanto a seconda
delle singole esigenze (tipologia di paziente, metodiche a
disposizione dell’operatore, grado di urgenza) può
e deve essere variato.
Terapia in attesa di espulsione spontanea
Nel 70% dei casi la colica renale è provocata da un calcolo
situato nell’uretere distale. Una terapia di attesa può
portare all’espulsione spontanea di più del 50%
dei calcoli, ma con una media del tempo di espulsione superiore
ai 10 giorni e con uso considerevole di analgesici, anche per
calcoli di dimensione inferiore ai 4 mm.
Inoltre si possono verificare alcune complicanze come infezione
delle vie urinarie, idronefrosi o coliche ricorrenti.
La probabilità che un calcolo ureterale venga espulso
spontaneamente dipende essenzialmente da una serie di fattori
“immodificabili” (dimensioni, sede, anatomia interna
dell’uretere, pregressa storia di espulsione spontanea)
e “modificabili” (spasmo, edema, infezione ureterale).
Obiettivi della terapia medica e farmaci studiati
L’obiettivo della terapia medica espulsiva dovrebbe essere
quello di prevenire i fattori modificabili e controllare la
sintomatologia dolorosa per favorire l’espulsione del calcolo.
In questi ultimi anni alcuni trial hanno proposto degli approcci
conservativi, avendo dimostrato l’efficacia di diverse
combinazioni farmacologiche nel favorire l’espulsione spontanea
dei calcoli ureterali distali.
Infatti, anche se il ruolo della terapia medica espulsiva nel
trattamento della calcolosi dell’uretere distale resta
ancora da chiarire, in questi studi si è ottenuta l’eliminazione
spontanea del calcolo in più dell’80% dei casi,
con un eccellente controllo del dolore.
Un tale approccio conservativo risulta inoltre proponibile per
calcoli di dimensioni fino a 10 mm, per un periodo massimo di
4 settimane, purché non insorgano deterioramento della
funzione renale, infezione o dolore intrattabile.
L’uso di farmaci si basa sulla dimostrazione a livello
dell’uretere umano della presenza di recettori alfa e beta
adrenergici: l’effetto stimolante sulla contrazione ureterale
è indotto dagli agonisti dei recettori alfa ed è
dose dipendente.
La noradrenalina ha un effetto cronotropo e inotropo positivo
sui recettori alfa, con aumento della frequenza della peristalsi
e del tono della muscolatura ureterale, fino a determinare,
ad alte dosi, la ostruzione ureterale totale. Per questo motivo
la stimolazione alfa-adrenergica riduce il flusso di urina ureterale.
Gli antagonisti selettivi dei recettori alfa-adrenergici diminuiscono
invece l’ampiezza e la frequenza della peristalsi ureterale,
con una diminuzione della pressione nel lume ureterale, e quindi
aumento della capacità di trasporto dei fluidi.
Successivamente è stata dimostrata la presenza nell’uretere
umano di sottotipi dei recettori adrenergici, gli alfa-1D.
Tra i farmaci testati e comparati, importanti risultati si sono
ottenuti con il tamsulosin, antagonista selettivo degli alfa1A-alfa1D
recettori adrenergici. La molecola aumenterebbe sia la pressione,
sia il flusso di urina a monte del calcolo, con riduzione della
pressione a valle; il contemporaneo rilassamento del collo vescicale
favorirebbe anche l’espulsione del calcolo migrato in vescica.
Inoltre tamsulosin permetterebbe di limitare l’uso di analgesici
poiché, diminuendo la frequenza delle contrazioni fasiche
peristaltiche nel tratto ureterale ostruito, si creerebbe una
riduzione dello stimolo algogeno. Paragonato ad altri alfalitici
non ha mostrato differenze statisticamente significative. Rispetto
a nifedipina e fluoroglucinolo (agente sintetico con lievi proprietà
anticolinergiche) ha dato risultati migliori, per tassi (97.1%)
e tempi di espulsione, riduzione di giornate lavorative perse;
inoltre ha permesso un trattamento domiciliare del paziente.
In un altro studio, al contrario, comparandolo alla nifedipina,
si ottengono risultati molto simili per quanto riguarda la percentuale
di espulsione e la necessità di terapia analgesica; il
tempo di espulsione risulta ridotto invece dal tamsulosin.
Usato da solo, come spasmolitico, aumenta il tasso di espulsione
spontanea e riduce tempo di espulsione, necessità di
ricovero e procedure endoscopiche, con un miglior controllo
del dolore rispetto al gruppo di controllo.
Altri farmaci che potrebbero essere impiegati sono i corticosterodi
e i calcioantagonisti, in genere associati, e il cui razionale
d’uso si spiega con le proprietà antiedemigene per
i corticosteroidi, e con l’attività spasmolitica
da parte dei calcioantagonisti.
Essi favorirebbero l’espulsione del calcolo, in tempi ridotti
e con minor uso di analgesici.
L’associazione di nifedipina e deflazacort favorisce, in
maniera statisticamente significativa, l’espulsione del
calcolo dell’uretere distale e riduce tempo di espulsione,
ricorso a FANS, numero di ricoveri e successivi interventi endoscopici.
L’uso di nifedipina va comunque effettuato con cautela
nei pazienti con ipotensione, angina, diabete e gravidanza.
L’uso di un cerotto a base di trinitrina (che agisce come
rilasciante ossido nitrico) non ha invece evidenziato alcun
significativo vantaggio, rispetto al placebo, per la espulsione
spontanea, tempo di espulsione del calcolo, uso di analgesici,
riduzione del dolore e interventi endoscopici.
|
|
|
|