M.D.
numero 2, 31 gennaio 2007
Pratica
medica
Da un edema agli arti inferiori alla diagnosi
di amiloidosi
di Tommaso Donvito - Medico di medicina generale, Gioia del
Colle (BA), AIMEF (in collaborazione con Antonio Pugliese
- Medico di medicina generale, Castellaneta (TA), Responsabile
Dipartimento Dermatologia AIMEF)
|
Un’assistita di 55 anni viene in ambulatorio nel mese
di settembre 2005 lamentando una spiccata astenia e la comparsa
di edema agli arti inferiori. La paziente soffre di insufficienza
venosa agli arti inferiori e in prima battuta collego i
sintomi alla calura estiva, ma ricordo che è da qualche
anno che seguo la sua elettroforesi, quindi controllo i
dati clinico-anamnestici in mio possesso. |
Storia
clinica
La
paziente è stata sottoposta ad appendicectomia all’età
di quattro anni. Soffre di sindrome ansioso depressiva reattiva
collegabile a problematiche familiari, malattia da reflusso
gastroesofageo, spondiloartrosi e vitiligine, oltre che alla
citata insufficienza venosa agli arti inferiori.
Dal 1999 è portatrice di una condizione di gammopatia
monoclonale di incerto significato (MGUS), tipizzata come IgG
lambda, per la quale ha effettuato, negli anni successivi e
fino all’anno precedente, i controlli ematochimici (ma
non con la prevista e consigliata periodicità), che hanno
attestato la sostanziale stazionarietà del quadro.
 Esame
obiettivo e ragionamento clinico
Esame
obiettivo e ragionamento clinico
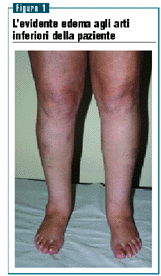
All’esame obiettivo rilevo le varicosità e le ectasie
capillari alle cosce e il vistoso edema a entrambe le gambe,
con fovea. L’edema fa assumere alle gambe un aspetto biancastro
che contrasta con quello scuro tipico delle insufficienze venose
croniche (figura 1).
Vista l’imponenza dell’edema e le caratteristiche
cliniche della paziente, ho escluso fra le possibili cause la
stasi venosa, la stasi linfatica e l'edema ortostatico.
In base alla visita ho escluso anche lo scompenso cardiaco e,
per l’aumentata permeabilità vascolare, allergie,
flogosi acuta, ecc.
Pertanto ho pensato agli edemi discrasici da ipoalbuminemia
e ho prescritto indagini ematochimiche mirate.
In effetti dagli accertamenti di laboratorio prescritti è
risultata una significativa e importante proteinuria (12 g/24
h), con riduzione delle proteine totali (5 g/dL) e con un
profilo elettroforetico tipico della sindrome nefrosica (riduzione
dell’albumina, aumento delle alfa-2 e riduzione delle gammaglobuline),
con funzionalità renale conservata e normale crasi ematica.
In base alla situazione clinica ho consigliato il ricovero ospedaliero
in ambiente nefrologico.
Prima diagnosi
All’ingresso in reparto vengono ripetute le indagini ematochimiche
e viene praticata una biopsia renale, che ha portato alla diagnosi
di sindrome nefrosica da glomerulonefrite a lesioni minime,
accompagnata dalla gammopatia monoclonale.
La paziente viene dimessa con la prescrizione di terapia con
prednisone alla dose di 75 mg/die.
Seconda diagnosi
Dopo due mesi prescrivo le indagini ematochimiche di controllo,
da cui si rileva la persistenza di proteinuria con valori sostanzialmente
inalterati rispetto all’esordio: 10 g/24 h.
Ricontatto i colleghi nefrologi i quali, visto il riscontro
di valori ancora alterati, riconsiderano in chiave critica e
retrospettiva il caso. La paziente viene nuovamente ricoverata.
Viene eseguita un’altra biopsia renale, che evidenzia la
presenza di deposito di fibre amiloidi a livello renale e quindi
viene posta la diagnosi di amiloidosi renale AL in gammopatia
monoclonale IgG lambda.
Contestualmente è stata eseguita una biopsia della cresta
iliaca oltre che un agoaspirato midollare che hanno portato
a conteggiare una plasmocitosi midollare del 20%.
Posta la diagnosi di amiloidosi e sapendo che ne sono stati
classificati più di venti tipi sulla base delle diverse
proteine precursori delle fibrille (proteine autologhe dovute
ad alterazioni del metabolismo e/o della conformazione), abbiamo
deciso di avviare la paziente presso il Centro per lo studio
e la cura delle amiloidosi sistemiche del Policlinico San
Matteo di Pavia.
Ricovero al Centro specialistico
La paziente è stata sottoposta al prelievo di cellule
staminali totipotenti dal suo midollo, poste in coltura e conservate.
Quindi ha iniziato terapia con agente chemioterapico melphalan
e desametasone ad alte dosi, da effettuare a cicli mensili
di 4 giorni ogni 28.
Decorso clinico
Sin dal primo ciclo la paziente ha presentato una spiccata mieloinibizione
indotta dal melphalan, con neutropenia (granulociti neutrofili
<1500/mm3) persistente ben oltre il previsto nadir del farmaco,
così da non riuscire a eseguire nei tempi prefissati
la terapia, se non riducendo la dose del farmaco (fino al 50%)
e allungando gli intervalli tra un ciclo e l’altro.
Al termine del quinto ciclo, pur essendosi normalizzato il livello
delle catene leggere nel siero, persiste elevata proteinuria
(18 g/24 h), con ipoprotidemia severa, all’elettroforesi
sierica: albumina 47.92, alfa-1 4.6, alfa-2 18.14, beta 18.63,
gamma 10.72; creatininemia 0.90 mg.
È stato deciso di sospendere il protocollo e di rivalutare
il caso. Questa evoluzione farebbe presupporre l’irreversibilità
del danno renale, anche se la normalizzazione del livello
delle catene leggere circolanti consentirebbe di pensare che
il clone plasmacellulare sia stato ridotto.
Conclusioni
L'amiloidosi deve essere considerata nella diagnosi differenziale
in caso di sindrome nefrosica non diabetica. Inoltre, alcuni
sintomi che talora possono presentarsi (aumento delle dimensioni
del fegato, ipotensione, perdita dell’appetito, calo
del peso corporeo, alterazione della sensibilità a mani
e piedi, diarrea) sono tipici di altre patologie di più
comune riscontro e di conseguenza è fondamentale che
siano correttamente interpretate dal Mmg.
La forma dell'amiloidosi AL è la più frequente,
con un'incidenza stimata di 0.8 per 100.000 persone/anno, seguita
dall'amiloidosi reattiva. Nonostante si accompagni a un clone
plasmacellulare neoplastico, questo tipo di amiloidosi si riscontra
in una ridotta percentuale di casi di mieloma multiplo.
La letteratura riporta che l'aspirato con ago sottile di grasso
periombelicale può sostituire la biopsia degli organi
coinvolti nella grande maggioranza dei pazienti con amiloidosi
AL sistemica.
Il follow up dopo chemioterapia viene realizzato con la quantificazione
delle catene leggere circolanti. Sebbene una remissione ematologica
completa sia auspicabile, una riduzione delle catene leggere
amiloidogeniche del 50-75% è spesso sufficiente a portare
a una stabilizzazione o regressione della disfunzione d'organo
e a un miglioramento della sopravvivenza.